Autor: Dr. Irina-Valentina Cojocaru, Msc, MBA
Indrumator: Conf. Univ. Dr. Mariana Cevei

Terapia in oncologie reprezinta o provocare pentru orice specialitate medicala sau auxiliara, datorita unicitatii fiecarui individ din punct de vedere genetic. Depasirea barierei de “cohorta” in perceptia cazurilor clinice si in atitudinea terapeutica este dificila, presupunand ca personalul medical si cel auxiliar sa aloce un timp mai indelungat studierii pacientului. De altfel, rezultatele bune necesita in general sacrificiu de timp si studiu, insa mediul de lucru actual si contextul economico-social limiteaza inaintarea pe aceste axe.
Conform NCI – National Cancer Institute din SUA, fondat in1937 de Presedintele F. D. Roosevelt, exista peste 100 de tipuri de cancer, in timp ce ASCO – American Society of Clinical Oncology mentioneaza peste 120 de tipuri. Cifrele impresioneaza mult mai mult, aplificate cu numarul de potentiali pacienti, estimat la nivel mondial de 23,6 milioane in anul 2030 si cu o rata de mortalitate pozitiva, respectiv 1.4% – 1.8% (raport datat 27.04.2018).
Parametrul cel mai important, urmarit in oncologie este “SPERANTA DE VIATA”, astfel ca toate actiunile intreprinse au ca scop cresterea sperantei de viata a pacientului. Al doilea parametru urmarit este QALY – quality adjusted life years sau QoL – quality of life, uneori renuntandu-se la interventii chirurgicale paleative in favoarea mentinerii “starii de bine” si calitatii vietii pacientului.
Terapia fizica actioneaza ca un vector pozitiv pentru ambii parametrii, cu cresterea mai importanta a calitatii vietii pacientului.
Mecanismele celulare ale degenerarii
Cancerul este o boala degenerativa, mecanismele de actiune fiind multiple. Declansarea este realizata de tumora in sine, urmata de cercuri vicioase ce includ efectele negative ale terapiei si comorbiditatile.
Tabloul pacientului roman care apleaza la servicii profilactice, in scopul prevenirii afectiunilor oncologice, reprezinta o persoana cu nivel intelectual ridicat, istoric familial relevant si/sau rezultat ce arata predispozitie genetica.
Descoperirile tumorilor in situ sunt rare, asigura de cele mai multe ori o rata de supravietuire mai mare, datorita initierii precoce a tratamentului. Raspunsul inflamator al pacientului este prezent inca de la inceput, amploarea acestuia fiind caracteristica fiecarei persoane. In circulatie sunt eliberate citokine specifice: TNF, IL-1, IL-6, IFN s.a.
Tumora in situ sau carcinom in situ – CIS reprezinta un grup de celule cu structura anormala sau diferita de celelalte celule tisulare locale, care prolifereaza necontrolat si care produc sau nu modificari adiacente cu aspect morfologic relevant. Binenteles, de-a lugul timpului, au fost identificate populatii de celule, morfologic straine de tesutul suport, care provin inca din timpul dezvoltarii embrionare, acestea nereprezentand mereu un trigger pentru celulele stem carcinogene. Binenteles, trebuie bine definit daca aceste celule straine reprezinta sau nu o tumora benigna.
Examinarea morfologica a elementelor celulelor tumorale trebuie corelata cu kinetica acestor celule. Anatomopatologul nu trebuie sa se limiteze la imagini statice pentru diagnostic, medicina de laborator moderna implica urmarirea celulelor timp indelungat, in conditii fiziologice si cuantificarea mecanismelor de actiune.
La noi in tara, cele mai cunoscute centre care pot oferi un diagnostic cu relevanta, inclusiv pentru tratamentul ulterior, sunt Transcend – IRO Iasi, Oncogen – SCJU Timisoara. Prin tehnicile moderne de laborator, poate fi definit profilul imunologic unic al pacientului, fapt ce va ajuta la instituirea terapiei anti-tumorale personalizate.
O celula, fie ea si tumorala, pentru a prolifera, trebuie sa reziste actiunii celulelor imunitare, am putea spune ca are nevoie de o „sanatate proprie”. Unele populatii de celule anormale sunt distruse de celulele K si NK, fara ca acest lucru sa fie resimtit. Autofagia este un alt mecanism prin care celulele tumorale pot fi distruse, in lipsa substratului energetic.
Celula tumorala este caracterizata, in principal, printr-un nucleu voluminos, modificari ale citoplasmei si elementelor citoplasmatice, prezenta filamentelor de actina si a microtubulilor ce ajuta in procesul de invazie. Elementul celular influentat cel mai mult de activitatea fizica este mitocondria tumorala. Mitocondriile celulelor tumorale ofera energia necesara multitudinii de mitoze. Doua procese majore sunt caracteristice mitocondriilor tumorale: glicoliza intensa la nivelul membranelor (Fenomenul Warburg) si deficitul de citocromoxidaza. De aceea, este bine ca in cazul in care hemoglobina inregistreaza scaderi la valori sub 10g/dL sa evitam administrarea de Fe pana la efectuarea unor investigatii complete, dar sa nu intrerupem exercitiile fizice. [1,3,4,5,17]
Celula tumorala utilizeaza ca substrat energetic cantitati mari de glucoza, pe care o converteste in acid lactic. Warburg a identificat in1924 un consum de 10 ori mai mare de glucoza, al celulelor tumorale in carcinomul hepatic, comparativ cu restul celulelor hepatice. Pentru fiecare molecula de glucoza metabolizata sunt eliberate 36 de molecule de ATP. Organismul incearca sa balanseze cererea de glucoza, pentru a intretine organele si functiile vitale, astfel ca, sursele de glucoza, in lipsa unui aport masiv vor fi, de prima intentie lipdele, urmate de afectarea metabolismului proteic. Rezultatul este acumularea la nivelul tesuturilor de radicali liberi de oxigen (ROS – specii reactive de oxigen), in diferite combinatii. [1,17]
O alta particularitate a celulelor tumorale este potentialul membranar foarte scazut, membrana externa fiind puternic ionizata negativ. [1,18]
In functie de tipul celulelor, tumorile se inscriu in 3 categorii: carcinoame (90%), limfoame si sacrcoame. Sarcoamele sunt cele mai rare, insa in recuperarea fizicala ocupa un loc important, datorita afectarii directe a aparatului kinetic, respectiv muschi, tesult fibros, oase, cartilaje. Este importanta efecturarea diagnosticul diferentiat cu fibromialgia !
Tumora matura este formata dintr-o multitudine de tipuri de celule, este o populatie foarte heterogena, semnalele REDOX (crosstalk) fiind transmise de la o celula la alta, raspunsul fiind diferit de la o celula la alta. Global insa, se inregistreaza o crestere a rezistentei la stress a populatiei tumorale.[1]
Tumorile maligne metastazeaza in intervale de timp variabile, astfel ca, daca tumora localizata nu a produs disfunctii locale sau disfunctii ale tesutului invadat, in mod sigur in faza de metastazare disfunctiile sunt resimtite de pacient, sub forma de manifestari nespecifice. Sunt recunoscute in medicina de specialitate imaginile cu metastaze, fara tumora localizata. Inca este studiata chemoatractia celulelor tumorale pentru diferite tesuturi in care metastazeaza si factorii ce pot bloca chemoatractantii, respectiv metastazarea osoasa este impresionanta si invalidanta in cancerul de prostata, dar inca nu stim de ce sunt atrase celulele tumorale acolo.
Incidenta metastazelor este direct proportionala cu marimea patului vascular din procesul de neoangiogeneza. Relatia dintre angiogeneza si fibroblastii asociati celulelor tumorale (CAFs) este intens studiata, aceasta avand un rol central in reglarea raspunsului imun si inflamatiei. CAFs sunt sursa importanta pentru IL6 si cresc rezistenta la agentii antitumorali.[4]
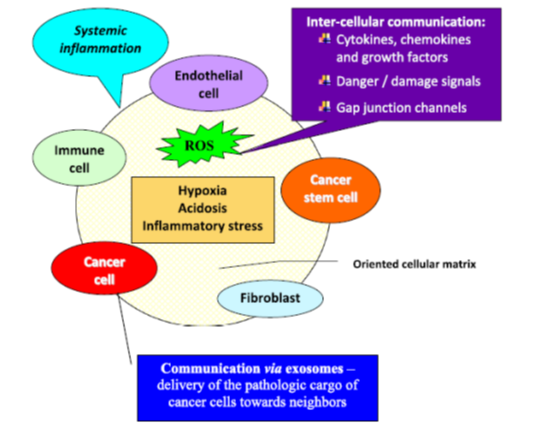
The redox biology network in cancer pathophysiology and therapeutics – Gina Manda, GheorghitaIsvoranu, Maria Victoria Comanescu, Adrian Manea, Bilge Debelec Butuner, KemalSami Korkmaz.[1]
Impactul psihologic
O lunga perioada dupa aparitia tumorii, pacientul este un om normal, apt sa desfasoare toate activitatile zilnice in care este angrenat.
Dupa aflarea diagnosticului, dimensiunea psihologica a problemei este preponderent a pacientului, pentru cei din jur nu se confrunta cu schimbari evidente. De aceea, diagnosticul trebuie comunicat in mod confidential, de o persoana abilitata, pentru diminuarea socului la aflarea vestii. Complianta pacientului la terapiile ulterioare este in directa relatie cu raspunsul emotional si acceptarea.
Pacientului diagnosticat cu cancer ii este amenintata o nevoie de baza, asa cum este descrisa de Maslow – nevoie de siguranta, de securitate.
Problematica ascunderii adevarului este vasta, aceasta abordare fiind inca practicata in Romania. Un rezultat negativ important al acestei abordari este amanarea tratamentului, lipsa de complianta si disciplina de viata a pacientului. Obtinerea Consimtamantului Scris din partea pacientului se poate transforma intr-o actiune imposibila.
Pe masura trecerii timpului si avansarii bolii, dimensiunea psihologica depaseste granitele pacientului, devine o dimensiune sociala a cercului de relatii. Pacientului i se atribuie eticheta de „victima”, fapt ce agraveaza starea de anxietate. Imposibilitatea efectuarii sarcinilor zilnice, datorita efectelor secundare ale tratamentului si fatigabilitatii, are un impact major asupra psihicului, in special in familiile in care exista copii.
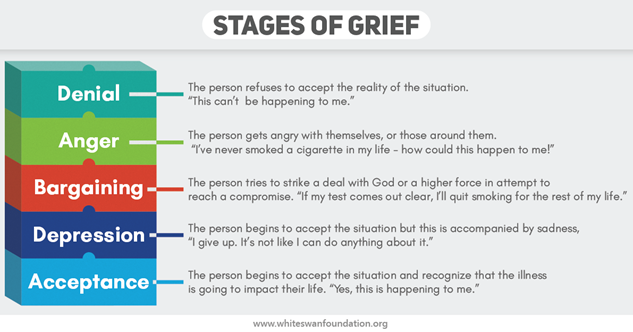
In cazul terapiilor curative, dar invalidante, pacientul se confrunta cu un nou scenariu-negarea: respingerea de catre societate, refuzul de a accepta situatia, refuzul de a se accepta pe sine, refuzul de a discuta cu persoane aflate in situatii similare.
Restrictiile alimentare, restrictiile pentru consumul de alcool, tutun, cofeina, tulburarile de gust, durerile, costul tratamentelor, disponibilitatea tratamentelor s.a. reprezinta vectori negativi care actioneaza asupra psihicului pacientului.
Intr-un comunicat de presa facut de ESMO in septembrie 2017 in Madrid, se arata ca efectele psihosociale ale terapiilor sunt mai importante ca efectele fizice, precum greata si varsaturile in timpul curelor de chimioterapie. Cele mai frecvente probleme sunt anxietatea si tulburarile de somn. Studiul s-a bazat pe feedback din partea pacientilor. Concluzia a fost ca exista diferente mari intre ceea ce considera medicii ca fiind important si ceea ce cred pacientii ca este important. (Patients Feel Psycho-social Impact of Chemo More Acutely Than Physical Side Effects).
De asemenea, impactul psihologic la aflarea vestii despre recurenta tumorii pare sa fie mai important, comparativ cu cel initial. (Oncology Nursing Society – Ferrell, Grant, Funk, Otis-Green, & Garcia, 1998; Vickberg, 2001; Sarna et al. ,2005).
Depresia va insoti pacientul de la aflarea vestii, pe toata perioada in care este considerat bolnav. Tratamentul medicamentos al depresiei se va face insa, doar in situatii grave, respectiv tendinta de suicid, atacuri de panica, violenta, orice actiune prin care pacientul isi poate face rau singur. Conform ESMO,9.8%-38.2% dintre pacientii dezvolta o boala psihica.
Directii de tratament
Echipa multidisciplinara este formata din: medic oncolog, chirurg oncolog, radioterapeut, asistenta de ingrijiri, psiholog, nutritionist, medic de recuperare medicala, fizioterapeuti, maseuri.
Directii de tratament:
- Tratament chirurgical curativ sau paleativ: chirugical. Post-chirurgical: analiza piesa biopsie, reconfirmare stadiu tumora
- Radioterapie [16]:
- Radioterapia externa 2D, 3D (teleterapia): tumori cerebrale, cancere ORL, cancer de prostata, cancer de san, cancere uterine, cancer esofagian, cancere pulmonare, cancer colorectal.
- Brahiterapia (curieterapia sau iradierea interna). Se poate combina cu radioterapia externa sau se foloseste ca unica metoda de iradiere.
- Radioterapia metabolica
- Radioterapia ghidata imagistic
- Radioterapia cu intensitate modulata (IMRT)
- Volumetric Modulated Arc Therapy – VMAT: tumori cerebrale, cancere ORL, cancer de prostata, cancer de san, cancere uterine, cancer esofagian, cancere pulmonare, cancer colorectal, cancer pancreatic, cancer de prostata, cancer de vezica, sarcoame, tumori cerebrale, limfoame.
- Radioterapia intraoperatorie
- Tomoterapia: iradiere in acelasi timp in locatii diferite
- Radiochirurgia şi radioterapia stereotactica (Stereotactic Radiosurgery şi Stereotactic Body Radiotherapy)
- Gamma Knife
- Cyberknife
- Protonterapia: tumori la baza craniului, la nivelul coloanei vertebrale, in vecinatatea globului ocular, parti moi
- Terapie fotodinamica
NOTA:
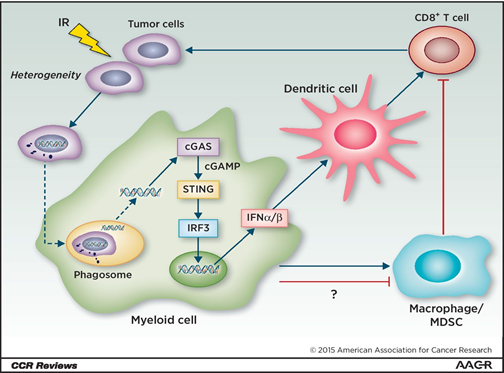
Speciile reactive de oxigen (ROS) afecteaza ADN-ul celular si stimuleaza proliferarea tumorala, insa pot fi utilizate si ca agenti terapeutici, acesta fiind pricipiul pentru radioterapie si terapia fotodinamica. Actiunea ROS tintita asupra celulelor tumorale duce la apoptoza acestora prin stress oxidativ, celulele tumorale avand un deficit de citocromoxidaza la nivelul mitocondriei. Astfel ca, efectele unor cantitati mari de ROS nu vor fi atat de citotoxice pentru celulele normale. Insa, actiunea radioterapiei asupra nucleului este mica, rezultand produsi de radioliza, precum electroni liberi si molecule instabile ce vor migra in fluidele aerobe formand compusi toxici. De asemenea, actiunea ROS prin terapie fotodinamica la 600 – 800nm este buna pe elementele citoplasmatice si la fel de saraca pentru nucleu. [1,3,20]
- Chimioterapie: terapia cu agenti tintiti, respetiv molecule mici ce pot fi intravazate in celula (tumori solide) si anticorpi monoclonali ce se leaga de membranele celulare (hemopatii maligne), inhibitori de tirozin-kinaza pentru leucemii, agenti imunomodulatori si inhibitoi proteazomici pentru mielom multiplu, inhibitori de histon-dezacetilaza pentru limfoame cutanate, agenti combinati pentru limfoame Hodgkin si anaplazice.
- Terapia hormonala: supresie androgenica, estrogenica
- Terapia nutritionala: nutritionistul stabileste dieta pacientului preoperator, postoperator si pe intreaga durata a bolii, in corelatie cu tipul de cancer, IMC, tipul de tratament, metabolismul bazal, efortul fizic. Restrictia principala este pentru glucide, insa se recomanda consum crescut de lichide.
- Psihoterapia: psihologul se ocupa de motivarea pacientului cu scopul cresterii compliantei la tratament, decide daca implicarea familiei este un factor pozitiv si stabileste gradul de discernamant al pacientului.
- Medicul de recuperare medicala: stabileste schema de recuperare in functie de tipul de tumora, localizare, grad, invalidanta sau nu, cu limitare kinetica sau nu, IMC, statusul cardiovascular, afectare pulmonara.
- Fizioterapeutii: evalueaza pacientii din punct de vedere al gradului de efort si al complexitatii exercitiilor, creeaza schema de exercitii pe care le pacientul le poate realiza la sala si la domiciliu, adapteaza programul in functie de sedintele de terapie – niciodata dupa chimioterapie, evalueaza complianta pacientului, monitorizeaza progresele si regresul. Fizioterapie antialgica, pentru revascularizare, pentru echilibrarea potentialelor membranare si pentru potentarea efectelor chimioterapiei, atunci cand este aplicata la nivelul tumorii.[18]
- Masoterapie: importanta pentru drenajul limfatic post mastectomie, pentru decongestionarea tesutului adiacent si fibrozat la nivelul cicatricilor postchirurgicale
- Administrarea de vaccinuri: HPV, imunostimulatoare
- Asistenta de ingrijiri urmareste complianta pacientului la tratament, alimentatia, eventualele leziuni aparute, severitatea efectelor adverse si indruma apartinatorii catre serviciile medicale specifice etc.
Mecanismele recuperarii prin exercitii fizice
In capitolul despre mecanismele celulare ale degradarii, am facut referire la consumul de energie al celulelor tumorale si particularitatile metabolice: glicoliza anaeroba, necesar crescut de glucoza, prezenta piruvatului si, in final, a acidului lactic ce este metabolizat in ficat etc. Toate aceste mecansime celulare sunt consumptive pentru organism si au ca rezultat diminuarea depozitelor strategice de energie. Organismul va disponibiliza rapid acizii grasi mononesaturati si polinesaturati pentru a produce energie imediata, dupa care va actiona prin disponibilizarea depozitelor de glicogen din muschi si transformarea in cliclul Krebbs in glucoza.
Pacientul oncologic resimte aceste transformari printr-o stare de fatigabilitate, somnolenta, tulburari de metabolism si slabiciune fizica. La pacientii obezi, dezechilibrele hidroelectrolitice sunt resimtite mai sever, obezitatea fiind in sine un factor de risc in oncologie. De asemenea, tesutul adipos este singurul care isi creste expresia in cancer, deoarece acizii grasi saturati raman cantonati si se acumuleaza in depozite.
In capitolul referitor la directiile de tratament, am mentionat importanta ROS – speciilor reactive de oxigen in procesele tumorale si antitumorale. Desi celulele tumorale au o mare capacitate de a se adapta la conditii diferite de hipoxie sau hiperoxie, prezenta ROS le face mai vulnerabile in conditiile unei cantitati crescute de oxigen si a presiuni crescute in reteaua noua de capilare formata. [1,20]
Efectele fiziologice ale exercitiilor fizice sunt cresterea patului vascular prin deschiderea mai multor capilare, datorita presiunii sangvine, cresterea oxigenarii sangelui, hipertermia, eliberarea in circulatie a unei cantitati crescute de celule K si NK, stimularea productiei la nivelul maduvei hematogene, avand ca rezultat imbunatatirea raspunsului imun.
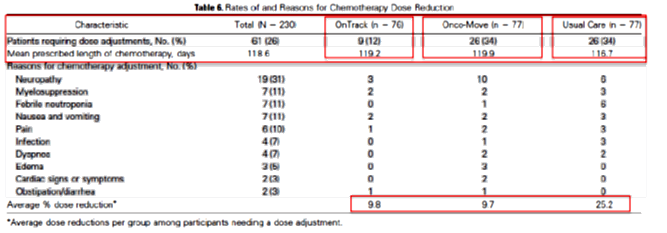
Exercitiile fizice potenteaza in acest fel efectul chimioterapicelor printr-o mai buna perfuzie, ajutand la intravazarea agentilor antitumorali si prin cresterea numarului de transportori de anticorpi monoclonali. Exista studii care au demonstrat cu cat poate fi redusa doza de chimioterapice in functie de gradul de efort usor, moderat sau crescut. Reducerea dozei de chimioterapice este in relatie directa cu scaderea reactiilor adverse ale acestor terapii.[6]

In cadrul radioterapiei, exercitiile fizice cresc nivelul de stres oxidativ la nivelul celulelor tumorale, astfel ca potenteaza efectele diferitelor tipuri de radioterapie.
Postchirurgical, exercitiile fizice ajuta pacientul la recapatarea mobilitatii, coordonarii, echilibrului si diminuarea durerii.
Deoarece cancerul este o maladie cu implicatii multiple la nivelul intregului organism, orice terapie noua a fost greu acceptata, inclusiv de lumea medicala. In cazul exercitiilor fizice, a existat teama ca acestea pot creste riscul de metastaze si pot epuiza pacientul. Cercetarea diferitelor tipuri de metasataze, a relevat insa faptul ca tumoretele nu sunt influentate in migrarea lor de exercitiile fizice, ci, in functie de tipul de celule, exista un patern si o chemoatractivitate ce nu pot fi influentate extern.
La nivel umoral, exercitiile fizice stimuleaza eliberarea de endorfine in circulatie, acestea actionand ca modulatori ai proceselor cognitive, crescand complianta pacietului prin conferirea starii de bine si reducand fatigabilitatea.
Un alt mit ce trebuie daramat, este cel al evitarii miscarii in afectiunilor pulmonare, pacientul cu cancer inregistrand o descrestere treptata a capacitatii functionale pulmonare. Spre diferenta de alte tumori cu localizari diferite, tumorile la nivelul plamanilor au celulele foarte bine adaptate nivelelor mai crescute de oxigen. In general aceste tumori sunt foarte rebele la tratamente, fibroblastii tumorali avand un rol central in protejarea acestor celule. Singurul tratament care poate creste insa capacitatea functionala a plamanului si totodata speranta de viata, este exercitiul fizic. In lipsa exercitiilor fizice, plamanul se deterioreaza mai mult, pacientul isi limiteaza activitatile zilnice si poate suferi atacuri de panica din lipsa aerului. Este nevoie ca fizioterapeutul sa educe pacientul cu privire la respiratia cadentata, metoda 5×5 si alte metode ce previn hiperventilarea. Binenteles, exercitiile trebuie urmarite foarte bine si stopate in momentul aparitiei dispneei sau cianozei.
Un alt impediment in efectuarea efortului fizic de-a lungul timpului, au fost metastazele si tumorile osoase. La nivelul acestor tesuturi exista un proces inflamator ce scade aportul de nutrienti prin limitarea circulatiei si aparitia compresiei, rezultatul fiind demineralizarea osoasa. Radioterapia accentueaza aceasta demineralizare, astfel ca demineralizarea nu este mereu localizata, ci poate afecta o suprafata mai mare. Teama in efectuarea exercitiilor fizice a reprezentat-o aparitia fracturii in os patologic. Insa, s-a demonstrat ca riscul de aparitie a fracturilor creste in cazul lipsei exercitiilor fizice. In concluzie, este bine ca acesti pacienti sa beneficieze de terapie fizica, prin exercitii active, cu evitarea izometriei. EMRI – Exercise Medicine Research Institute din Australia a demonstrat ca incarcarea mecanica a oaselor, reduce dramatic osteoliza si procesul de formare a tumorii si creste masa oaselor prin ingrosare trabeculara.
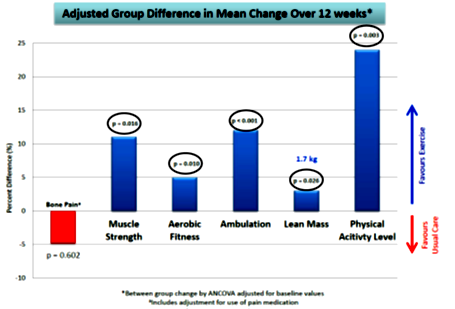
Exercise Medicine Research Institute
Efortul fizic sustinut (heavy exercise) duce la consum de glucoza, fapt care ajuta la diminuarea disponibilului de glucoza pentru celulele tumorale si intr-un final la autofagie. Acest tip de efort este bine sa fie combinat cu „infometarea” (starvation) pana la limita de suportabilitate a pacientului. Pierderea in greutate datorata exericiilor fizice sustinute, este un element pozitiv pentru persoanele obeze.[5,8]
Exercise Medicine Reseach Institute din SUA a efectuat o metaanaliza pentru 26 de studii referitoare la mortalitatea specifica in cancerul de san, cancerul de prostata si cancerul colorectal, rezultatul fiind o medie de 37% pentru reducerea mortalitatii specifice la pacientii care urmeaza un program de exercitii fizice. De asemenea, au observat o reducere a mortalitatii specifice la pacientii cu tumori recurente, inscrisi intr-un program de recuperare fizica.
Exista diferente in tolerarea efortului fizic in functie de varsta si trebuie tinut cont de problematica comuna a pacientilor de varsta a 3-a. Intr-un articol publicat in 2016 sub egida ESMO, se afirma ca incidenta de aparitie a cancerului este de 11 ori mai mare dupa varsta de 65 ani, acesti pacienti, spre deosebire de cei tineri, fiind mai toleranti la durere. Directiile de terapie sunt conservatoare la acesti pacienti, punand accentul pe cresterea calitatii vietii pacientilor. Raspunsurile la chimioterapie si radioterapie sunt diferite la acesti pacienti, non-efective comparativ cu cei tineri. Leziunile dupa sedintele de radioterapie sunt mai importante la acesti pacienti, datorita scaderii cantitatii de colagen in tesuturi si deshidratarii. Aceste leziuni pot limita perioadele de exercitii fizice.
Recuperarea metabolica si nutritionala
Exista mai multe teorii referitoare la dieta pacientilor cu cancer, in functie de stadiul tumorii si de comorbiditatile asociate. Terapia prin nutritie are un rol foarte important in orice afectiune medicala, in ultimii ani dezvoltandu-se ca ramura medicala si fiind sustinuta foarte mult de industria farma.
In spitalele din Romania a fost creata functia de Director de Ingrijiri, aceasta fiind persoana responsabila inclusiv cu verificarea dietei pacientilor.
Terapia nutritionala a devenit o preocupare comuna a tuturor oamenilor, urmand sintagma „suntem ceea ce mancam”. Se remarca in ultimii ani oferta foarte complexa de suplimente alimentare, suplimente naturale si produse bio. Aceasta atitudine nu ajuta foarte mult terapeutul, pacientul cu cancer fiind adesea prins in capcana reclamelor si a solutiilor miraculoase. O parte din suplimentele alimentare si din alimente interactioneaza cu chimioterapicele, scazand actiunea acestora prin mecanisme de blocare. Din pacate, situatiile sunt inevitabile si este nevoie ca nutritionistul sa investeasca mai mult timp in consilierea pacientului, nu doar sa emita schema nutritionala.
Lipsa educatiei in alimentatie este o problema globala, ce trebuie rezolvata atat in scoala primara cat si prin cursuri pentru parinti. Dezechilibrele alimentare favorizeaza dezvoltarea ulterioara a bolilor, cresc riscul de obezitate, malnutritie si sunt generatoare de stress.
Ca sprijin in evaluarea statusului nutritional al pacientului au fost dezvoltate instrumente de catre companiile farmaceutice implicate in productia de nutritie clinica.
Obiectivul terapiei nutritionala in cancer este scadereaingestiei de glucoza sau glucoformatori, pentru a reduce suportul energetic alcelulelor tumorale (Starvation). Binenteles, prin mecanisme metabolice, orice substrat nutritional poate fi transformat in glucoza, insa cu un cost de timp mai mare.
Datorita catabolismul proteic accentuat, se instaleaza slabiciunea musculara si, de cele mai multe ori, atitudinea medicului oncolog este de a recomanda pacientului consum crescut de proteine. Medicul oncolog, in lipsa unui nutritionist, poate fi responsabil de dieta pacientului. De asemenea, medicul de recuperare medicala poate sa indice suplimentarea cu proteine pacientilor cu slabiciune fizica.
S-a demonstrat insa ca infometarea combinata cu efort fizic sustinut este unul dintre mecanismele cele mai eficiente in distrugerea tumorilor. Pentru atingerea acestei performante, nutritionistul trebuie sa colaboreze cu psihologul, familia si cercul de relatii. Este un proces mental de mare determinare prin care trebuie sa treaca pacientul, renuntand nu doar la obiceiurile alimentare, ci confruntandu-se cu senzatia de foame. Insa nu este imposibil !
Urmarind mecanismul fiziologic, descoperim insa o serie de particularitati in metabolizarea nutrientilor. La capitolul referitor la mecanismele celulare ale degradari, am mentionat ca statusul inflamator apare odata cu tumora. La nivelul intestinului se afla localizate 80% din celulele care secreta anticorpi si care devin deficitare prin 2 mecanisme: mecanismul consumtiv prin productia exagerata de anticorpi si mecanismul de deprivare nutritionala, prin afectarea vascularizatiei la nivelul intestinului, in special in terapiile de infometare. La nivelul vililor intestinali, zona apicala este prima afectata in cazul lipsei alimentatiei, aceasta fiind si zona de absorbtie a proteinelor. Alternarea perioadelor de infometare cu dieta hiperproteica are eficienta redusa, deoarece provocam pacientului tulburari de tranzit ce antreneaza electrolitii si provoaca deshidratarea.
Dupa perioada de infometare, reluarea alimentatiei se face treptat, cu formule enterale pe baza de aminoacizi si peptide, izocalorice si in cantitati de adaptare pornind de la 20 kCal si ajungand in prima zi la portii de 100 kCal, fara depasirea de 500 kCal in total. Daca pacientul tolereaza bine dieta, in interval de 3 zile trebuie sa se ajunga la portii de 200 kCal la o masa, 4-5 mese pe zi. Trecerea la dieta hipercalorica hiperproteica, cu proteine intregi si hidrolizate se face incepand cu a 2-a saptamana, putand sa ajungem de la 1.3 kCal/ml pana la 2kCal/ml. Formulele alese trebuie sa fie sarace in glucide si destinate pacientilor cu cancer. Principalele produse de acest tip, utilizate in Romania, sunt: Nutricomp Peptid, Nutrison Advanced Peptisorb, Supportan, Fresubin Protein Energy Drink, Nutrison Protein Plus Multifibre. Avantajul utilizarii nutritiei enterale este atat al pacientului, cat si al medicului, deoarece exista o cantitate controlata de nutrienti ce poate fi monitorizata. Proteinele sunt extrase in principal din zer si au inalta valoare biologica. Lipidele folosite sunt PUFA si MUFA care au avantajul de a nu creste valoarea colesterolului in sange. Glucidele sunt de tipul maltodextroza. Fibrele sunt extrase majoritar din mazare. Dietele sunt imbogatite cu antioxidanti.
Sindromul anorexie – casexie reprezinta un cer vicios intretinut de tumora si de tratamentul antitumoral. Anorexia este data de infometarea prelungita, intoleranta la diferite alimente, modificarile de gust, miros si varsaturile care apar in timpul tratamentelor. Dupa cum mentionam mai sus, celulele mucosei intestinale sunt afectate de lipsa alimentatiei, absorbtia proteinelor fiind prima afectata, urmata de absorbtia lipidelor. Glucidele se misca liber prin membrane. Casexia reprezinta o urgenta medicala, aceasta fiind prezenta in multe afectiuni cronice in stadiul terminal sau in cazul persoanelor cu boli metabolice sau subnutrite. In cancer, casexia apare datorita afectarii metabolismului proteic prin scaderea anabolismului la nivelul ficatului si catabolismului proteic accentuat la nivel muscular, prin proteoliza fiind obtinuta glucoza. Functia renala este afectata datorita compusilor toxici prezenti in urma terapiilor antitumorale, precum si a corpilor cetonici rezultati in urma procesului de neoglucosinteza, astfel ca exista un clearence deficitar. Afectarea metabolismului proteic, conduce la afectarea metabolismului lipidic, lipoliza fiind stimulata de factori tumorali inductori si modulatori. Sindromul anorexie-casexie apare mai frecvent la cancerele din zona ORL si sistemul digestiv. Sunt impresionanate manifestarile din cancerul pancreatic, cand exista afectare de procesare a majoritatii nutrientilor asociata cu dureri foarte mari si prognostic negativ. [10,16]
La reluarea alimentatie trebuie tinut cont de pacientii diabetici, diabetul aparand de novo la aproximativ 40% dintre pacientii diagnosticati cu cancer.
O alta atentie deosebita trebuie acordata tipului de proteine, deoarece trebuie excluse produsele care contin glutamina sau produsele care contin proteine din soia si alte plante.
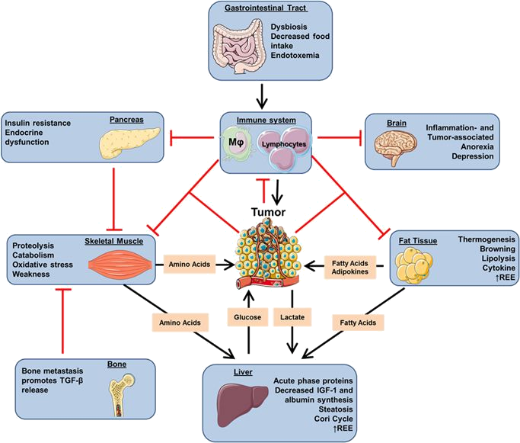
Understanding cachexia as a cancer metabolism syndrome, https://www.nature.com/articles/oncsis20163#auth-1
La pacientii cu tumori avansate, atitudinea terapeutica este de a creste calitatea vietii, astfel ca restrictiile alimentare sunt mici. De asemenea, administrarea de vitamine la aceasti pacienti nu este restrictionata, consderandu-se ca beneficiile globale sunt mai mari decat impactul asupra tumorii.
Pentru pacientii la care reluarea alimentatiei se face pe sonda nazogastrica, nazojejunala si stoma exista diete ce trebuie administrate cu ajutorul pompelor de nutritie. Este posibil ca acesti pacienti sa se alimenteze toata viata prin aceste dispozitive, acest lucru avand un impact psihosocial major.
Binenteles, dupa reluarea alimentatiei, pacientul va dori sa consume alimente normale, fapt ce nu ajuta foarte mult, deoarece toate produsele contin glucide, inclusiv carnea. Trebuie explicate aceste lucruri, inclusiv familiei si, trebuie configurat un regim alimentar combinat cu nutritie enterala. Pentru oferirea unei alternative cautarilor si leacurilor miraculoase, nutritionistul poate orienta pacientul catre terapia holistica, insa cu mentiunea ca presupune costuri ridicate.
Recuperarea psiho-sociala
Recuperarea psiho-sociala a pacientului oncologic, incepe imediat dupa anuntarea diagnosticului, deoarece starea emotionala a pacientului influenteaza relatiile familiale si cele la locul de munca.
Dupa cum mentionam la inceputul lucrarii, pacientul diagnosticat de timpuriu cu cancer, poate duce o viata normala o lunga perioada de timp, ceea ce il face apt de munca. Medicul oncolog, impreuna cu psihologul trebuie sa incurajeze pacientul sa nu intrerupa munca, deoarece s-a demostrat ca pacientii angrenati in activitati profesionale suporta mai usor tratamentul, se reintegreaza mai usor in cazul opririi temporare a muncii si au o motivatie mult mai buna in urmarea tratamentelor.
Totusi, exista tipologii diferite si persoane care nu depasesc bariera psihologica a bolii. O serie de tulburari bipolare pot sa aiba ca punct de initiere socul aflarii diagnosticului.
Implicarea pacientilor in activitati casnice zilnice ajuta, dar nu suficient, deoarece pacientul este tentat sa-si creeze o zona de confort pe care sa nu o mai paraseasca usor. Zona de confort, cum o numesc psihoantropologii sau zona de siguranta este caracteristica fiecarui om, parasirea acestei zone necesitand o motivatie importanta. De exemplu, zona de confort a adolescentilor poate fi parasita in momentul in care nevoile materiale depasesc posibilitatile parintilor, acestia cautand un loc de munca. Zona de confort a pacientilor oncologici insa, nu este una proactiva, fapt ce afecteaza viata familiei.
In SUA si Australia se practica terapia de grup, pacientii fiind incurajati sa interactioneze cu alti pacienti cu afectiuni similare, in prezenta unui moderator. Interactiunea cu „locuitorii din noua lume” il ajuta pe pacient sa depaseasca sentimentul de solitudine, de abandon, pesimismul, interiorizarea.
In Romania acest tip de interactiune se realizeaza in spitale si este bine sa tinem cont, cel putin la inceput, de colegii de salon ai pacientilor cu stari emotionale negative. Oricum, felul comunicativ al romanilor in general, ajuta in depasirea barierelor psihice.
Pacientul poate invata de la alti pacienti ce sa faca pentru a-si imbunatati starea emotionala, pentru a depasi durerea si efectele adverse ale tratamentelor.
Rolul medicinei de recuperare este foarte important, exercitiile fizice crescand nivelul de endorfine, reducand durerea si conferind o stare de bine. Fizioterapeutul poate recomanda pacientului o serie de exercitii ce pot fi facute la domiciliu. De asemenea, in cadrul Terapiei Ocupationale pacientii invata activitati pe care le pot face acasa si sunt sfatuiti sa caute profesii adecvate. In acest scop, pacientii pot fi evaluati cu ajutorul schemelor ocupationale.
In Jurnalul American de Terapie Ocupationala este prezentat cazul unui barbat in varsta de 38 ani, diagnosticat cu limfom non-Hodgkin tratat prin transplat cu celule stem allogene, evaluat conform tabelului de mai jos.
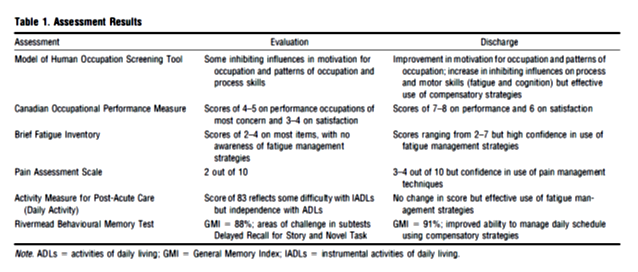
In urma acestor testari si a interviului cu pacientul, terapeutul a stabilit obiectivele terapiei ocupationale, astfel: 1. focusul principal este de a-l educa pe pacient sa-si gestioneze singur fatigabilitatea si disfunctiile cognitive, sa-si mentina activitatea fizica la nivelul partii superioare a corpului pentru realizarea cat mai buna a miscarilor si sa urmareasca simtomele rejectiei de grefa (GVHT); 2. Implicarea in activitati eliberatoare de stress; 3. Sustinerea informationala cu privire la medicina integrativa si complementara, in completare la medicina traditionala. [23]
Din saptamana a 12-a dupa transplant, terapeutul a efecuat 2 sedinte de TO pe saptamana, timp de 8 saptamani, dupa care a fost mentinuta 1 sedinta pe saptamana. Sedintele au inclus metode de conservare a energiei, descoperirea metodelor de rezolvare a sarcinilor, strategii de reducere a anxietatii si depresiei prin exercitii de implicare mentala profunda, strategii pentru imbunatatirea somnului, yoga si compozitii artistice in scris, invatarea unor metode de combatere a oboselii acasa. (Occupational Therapy Interventions for Adults With Cancer, Brent Braveman, Elizabeth G. Hunter, Jennifer Nicholson, Marian Arbesman, Deborah Lieberman).[23]
Familia si cercul de relatii sunt foarte importante, acestia trebuie sfatuiti sa caute activitati de divertisment in care poate fi implicat pacientul si sa incurajeze orice idee ar putea sa-l scoata pe pacient din zona de confort.
Pentru evaluarea psihologica a pacientului, se pot utiliza diferite teste de screening, precum Distress Thermometer, Edmonton Symptom Assessment System (ESAS) in care pacientul indica singur pe o scara de la 0 la 10 eventualele nevoi sau probleme, Anxiety Depression Scale (HADS) si Brief Symptom Inventory (BSI), insa nimic nu poate echivala valoarea discutiei directe cu pacientul. (Advancing psychosocial care in cancer patients, Luigi Grassi, Conceptualization, Methodology, Writing – Original Draft Preparation,a,1,2 David Spiegel, Writing – Review & Editing,3 and Michelle Riba, Writing – Review & Editing4,5) [21,23]
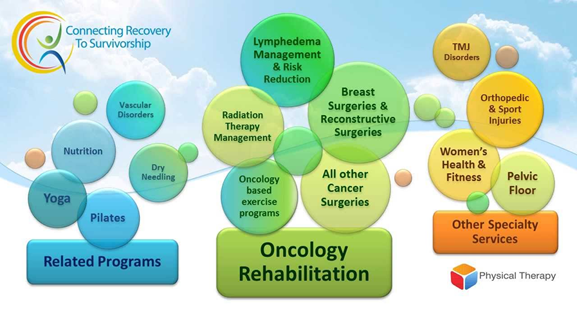
Ghiduri internationale – recomandari pentru recuperarea fizica
In 2017, R. Segal si col. au publicat in Revista Current Oncology Practice Guideline „Exercise for people with cancer: a clinical practice guideline”. In scopul elaborarii acestui ghid, au fost integrate informatiile din 3 ghiduri cu 18 review-uri si 29 de studii randomizate. Ghidul elaborat contine recomandari referitoare la durata, frecventa si intensitatea exercitiilor pentru bolnavii de cancer. Concluzia este ca exista suficiente dovezi care arata beneficiile terapiei fizicale in oncologie, atat pe durata bolii, cat si ulterior. Ghidul este elaborat pentru Canadian Society for Exercise Physiology.[15]
Recomandari:
- Persoanele bolnave de cancer pot efectua un numar moderat de exercitii fizice, in depline conditii de siguranta, in timpul tratamentului si dupa terminarea acestuia. Exercitiile fizice sunt recomandate pentru imbunatatirea calitatii vietii QoL persoanelor bolnave de cancer.
- Clinicienii trebuie sa sfatuiasca pacientii sa aiba un program consistent de exercitii fizice, cu recomandarea Canadian Society for Exercise Physiology si a American College of Sports Medicine (http://www.csep.ca/en/guidelines/guidelines-for-other-age-groups). Mai jos sunt recomandarile pentru durata, fecventa si intensitate:
■ Un target de 150 minute de exercitii aerobice cu intensitate moderata, pe perioada de 3-5 zile si exercitii pentru cresterea rezistentei la efort, cel putin de 2 ori pe saptamana.
■ Exercitiile pentru cresterea rezistentei la efort trebuie sa implice grupele mari de muschi, de 2-3 ori pe saptamana (8–10 grupe musculare, 8–10 repetari, 2 seturi).
■ Fiecare sedinta trebuie sa includa etapele de incalzire si revenire dupa efort.
3. O evaluare inainte de inceperea exercitiilor pentru identificarea efectelor bolii, tratamentelor si comorbiditatilor asociate este recomandata pentru toti pacientii cu cancer. (Pre-exercise assessment).
4. Este recomandat ca, unde este posibil, ca pacientii bolnavi de cancer sa efectueze exercitiile in cadrul unui grup sau sub supraveghere, pentru ca interactiunea cu mediul inconjurator poate oferi un beneficiu suplimentar sau crestere a QoL si calitatea exercitiilor este mai buna.
5. Este recomandat ca, unde este posibil, bolnavii de cancer sa faca exercitiile la o intensitate moderata ( de 3-6 ori mai mult decat efortul normal), si sa transforme acest lucru intr-un mod de viata, ceea ce ar duce la rezultate pozitive pe termen lung asupra QoL si a conditiei fizice.
American College of Sports Medicine orgnizeaza cursuri de certificare pentru ACSM/ACS Certified Cancer Exercise Trainer (CET).
In 2017, in Journal of Functional Morphology and Kinesiology a fost publicat „Clinical Implementation of Exercise Guidelines for Cancer Patients: Adaptation of ACSM’s Guidelines to the Italian Model”. Autorii au identificat problematica legata de tratament, precum si comorbiditatile asociate: limfedem, neuropatie, tulburari metabolice. Fata de ghidurile prezentate mai sus, se insista pe importanta exercitiilor pentru imbunatatirea respiratiei si circulatiei – cardiorespirator fitness CRF, acestea scazand riscul decesului prematur. De asemenea, un capitol este rezervat terapiei nutritionale.[19]
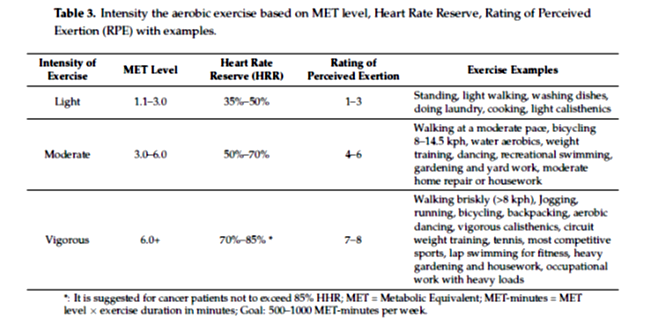
De asemenea, targetul activitatii fizice pentru pacienti post-tratament este de 500 – 1000 METS minute de activitate pe saptamana. Pentru atingerea acestui target, pacientul trebuie aloce minim 150 minute/saptamana pentru exercitii deintensitate moderata sau 75 minute pe saptamana, de efort fizic sustinut. Intensitatea exercitiilor trebuie sa se se coreleze cu o crestere a VO2 max de 40- 60% si cu o frecventa cardiaca de rezerva, definta ca diferenta dintre fecventa cardiaca maxima si frecventa cardiaca bazala.
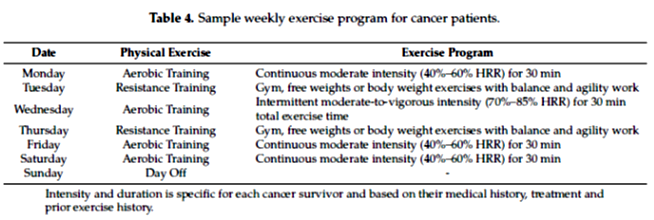
Programul de exercitii al unuipacient care a fost sedentar, trebuie sa inceapa cu exercitii usoare, dupa care sa fie crescuta intensitatea exercitiilor.
Trainingul de rezistenta anaeroba este foarte util in cazul pacientilor cu afectari la nivelul oaselor si afectari neuromusculare. Se apreciaza ca forta unui bolnav de cancer poate fi crescuta in medie cu 20 – 50% prin efectuarea exercitiilor de intarire a musculaturii. Corectarea viciilor de postura este un obiectiv de recuperare, mai ales pentru faptul ca majoritatea pacientilor sunt trecuti de 50 de ani. De asemenea, exercitiile de echilibru sunt importante si ca exemplu, autorii mentioneaza exercitiile cu cate un picior pe placa de echilibru. Exercitiile de stretching (pilates) trebuie sa faca parte din rutina zilnica, pentru cresterea flexibilitatii/mobilitatii.
Tabelul urmator reprezinta contraindicatiile pentruefectuarea exercitiilor, conform acelorasi autori:
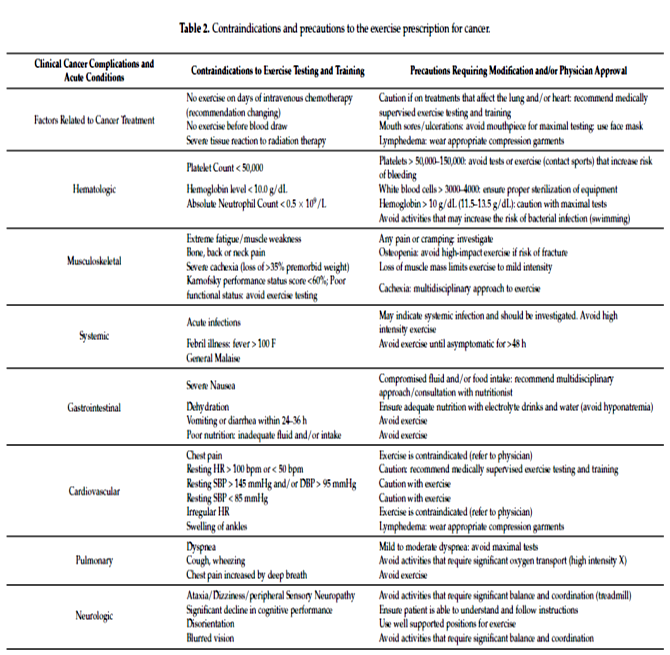
Recomandarile din ghidurile Societatii Europene de Oncologie Medicala (ESMO) sunt cele aplicabile in Romania, sunt traduse si pot fi descarcate de pe website-ul Ministerului Sanatatii. ESMO accepta recomandarile urmatoarelor ghiduri: Exercise and Sport Science Australia, Comprehensive Cancer Center the Netherlands, the German Cancer Association, and the British Association of Sport and Exercise Science. De asemenea, subliniaza importanta recomandarilor elaborate de ACSM si le adopta.
ESMO cuprinde in recomandarile de tratament pentru diferite tipuri de cancer, indicatii pentru programe de exercitii fizice. De asemenea, exista ghiduri elaborate impreuna cu alte societati medicale europene, respectiv ESMO-ESGO-ESTRO pentru cancerul endometrial, ESMO – ESSO – ESTRO pentru cancerul anal, care mentioneaza exercitiile pelvine pe podea s.a. [12,13,14]
Pentru cancerul de san, care ocupa primul loc in lista incidetei in populatia genarala, se mentioneaza foarte clar ca limfedemul nu reprezinta o contraindicatie pentru exercitii si, in plus, femeile cu limfedem post-mastectomie au voie sa lucreze cu greutati pentru intarirea musculaturii superioare a corpului. In cazul formelor rebele de cancer la san, la femeile sub 40 de ani, exercitiile fizice sunt recomandate zilnic, cel putin 150 minute pe saptamana, de activitate moderata.
Bibliografie
- The redox biology network in cancer pathophysiology and therapeutics, Gina Manda,Gheorghita Isvoranu, Maria Victoria Comanescu, Adrian Manea, Bilge Debelec Butuner,Kemal Sami Korkmaz, http://dx.doi.org/10.1016/j.redox.2015.06.014.
- Exercise Medicine for Cancer Management, Rob Newton PhD, AEP, CSCS*D, Exercise MedicineResearch Institute, Australia.
- Oxidative Therapy Against Cancer, Manuel de Miguel and Mario D. Cordero, Departamento de Citología e Histología Normal y Patológica, Facultad de Medicina, Universidadde Sevilla, Sevilla, Spain.
- RBC-ATP Theory of Regulation for Tissue Oxygenation-ATP Concentration Model, Terry E.Moschandreou, Additional information is available at the end of the chapter http://dx.doi.org/10.5772/48580.
- Oxidative Stress and Antioxidant Defenses Induced by Physical Exercise, Juana M.Morillas-Ruiz and Pilar Hernández-Sánchez, Additional information is availableat the end of the chapter, http://dx.doi.org/10.5772/61547.
- The Role of Exercise in Chemotherapy-Induced Peripheral Neuropathy, Karen Y. Wonders andBrittany Stout Additional information is available at the end of the chapter http://dx.doi.org/10.5772/62839.
- Physical Therapy in Patients with Cancer, Shinichiro Morishita and Atsuhiro Tsubaki,Additional information is available at the end of the chapter, http://dx.doi.org/10.5772/67286.
- Understanding Cachexia, Sarcopenia, and Physical Exercise in Patients with Cancer, Shinichiro Morishita, Atsuhiro Tsubaki and Jack B. Fu, Additional information is availableat the end of the chapter http://dx.doi.org/10.5772/67628.
- What’s New Among Cancer Etiology Horizon? Trinanjan Basu, Additional information isavailable at the end of the chapter, http://dx.doi.org/10.5772/intechopen.71305.
- Nutrition and Physical Activity During and After Cancer Treatment: An American Cancer Society Guide for Informed Choices, CA Cancer J Clin2006;56;323-353.
- Statistics fact sheet, Fact sheet last updated December 2017, EXTERNAL VERSION, Macmillan Cancer Support.
- ESMO-ESGO-ESTRO Consensus Conference on Endometrial Cancer: diagnosis, treatment and follow-up,Annals of Oncology 27: 16–41, 2016, doi:10.1093/annonc/mdv484.
- ESO-ESMO 3rd international consensus guidelines for breast cancer in young women (BCY3),The Breast 35 (2017) 203e217.
- Anal cancer: ESMO-ESSO-ESTRO Clinical Practice Guidelines for diagnosis, treatment and follow-up, Annals of Oncology 25 (Supplement 3): iii10–iii20, 2014,doi:10.1093/annonc/mdu159, Published online 6 July 2014.
- Exercise for people with cancer: a clinical practice guideline, R. Segal md, C. Zwaalmsc, E. Green rn, J.R. Tomasone phd, A. Loblaw md msc, T. Petrella md, and the Exercise for People with Cancer Guideline Development Group, Curr Oncol. 2017Feb;24(1):40-46.
- Concepte actuale de ingrijire a pacientului oncologic si noi metode terapeutice, autor Dr. Delia Mateescu, 2014
- Metabolic Pathways of the Warburg Effect in Health and Disease: Perspectives of Choice,Chain or Chance, Jorge S. Burns 1,2,* and Gina Manda 3, International Journalof Molecular Sciences, 2017.
- Electrotherapy on Cancer: Experiment and Mathematical Modeling, Ana Elisa Bergues Pupo1,Rolando Placeres Jiménez2 and Luis Enrique Bergues Cabrales3, Brasil, Cuba, AnaElisa Bergues Pupo, Rolando Placeres Jiménez and Luis Enrique Bergues Cabrales(2011), http://www.intechopen.com/books/current-cancer-treatment-novel-beyond-conventionalapproaches/electrotherapy-on-cancer-experiment-and-mathematical-modeling.
- Clinical Implementation of Exercise Guidelines for Cancer Patients: Adaptation of ACSM’s Guidelines to theItalian Model, Laura Stefani 1,*, Giorgio Galanti 1 and Riggs Klika 2, J.Funct. Morphol. Kinesiol. 2017, 2, 4; doi:10.3390/jfmk2010004
- Essential Role for Oxidative Phosphorylation in Cancer Progression, Maria Chiara Maiuri andGuido Kroemer, Cell Metabolism 21, January 6, 2014, http://dx.doi.org/10.1016/j.cmet.2014.12.013.
- The Psychosocial impact of Cancer on the Individual, Family, and Society, LINDA M. GORMAN, RN, MN, APRN, BC, OCN®, CHPN, Copyright by OncologyNursing Society. All rights reserved.
- Starvation,Stress Resistance, and Cancer, Roberta Buono and Valter D. Longo, Trends in Endocrinology & Metabolism, April 2018, Vol. 29, No. 4 https://doi.org/10.1016/j.tem.2018.01.008.
- Occupational Therapy Interventions for Adults With Cancer, Brent Braveman, Elizabeth G. Hunter, Jennifer Nicholson, Marian Arbesman, DeborahLieberman, The American Journal of Occupational Therapy, September/October2017, Volume 71, Number 5.
- www.clinicanera.ro
